1.
某小组比较Cl-、Br-、I- 的还原性,实验如下:
| 实验1 | 实验2 | 实验3 | |
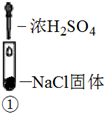
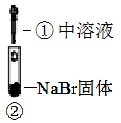
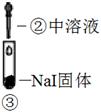
| 装置 | | | |
| 现象 | 溶液颜色无明显变化;把蘸浓氨水的玻璃棒靠近试管口,产生白烟 | 溶液变黄;把湿KI淀粉试纸靠近试管口,变蓝 | 溶液变深紫色;经检验溶液含单质碘 |
下列对实验的分析不合理的是( )
A.
实验1中,白烟是NH4Cl
B.
根据实验1和实验2判断还原性:Br->Cl-
C.
根据实验3判断还原性:I->Br-
D.
上述实验利用了浓H2SO4的强氧化性、难挥发性等性质
【考点】
卤素原子结构及其性质的比较;
基础巩固
能力提升
拓展培优