1.
工业产生的废气COX、NOX、SOX 对环境有害,若能合理的利用吸收,可以减少污染,变废为宝.
(1)
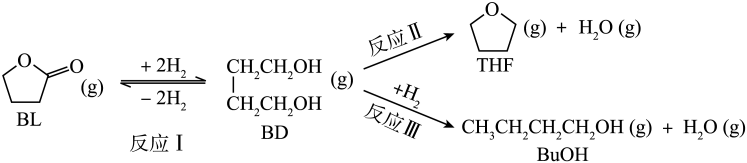
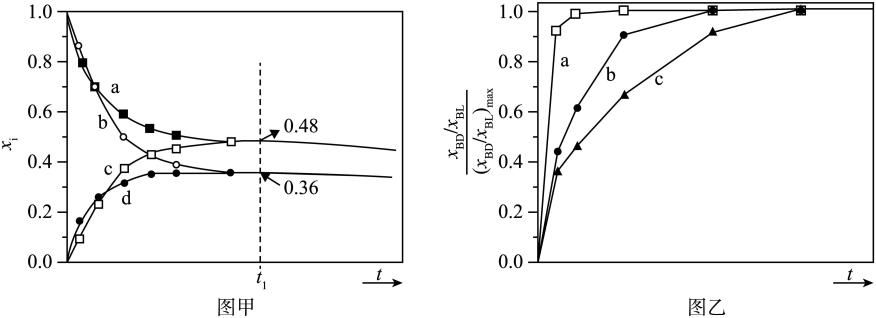
有一种用CO2生产甲醇燃料的方法:CO2+3H2⇌CH3OH+H2O
(2)
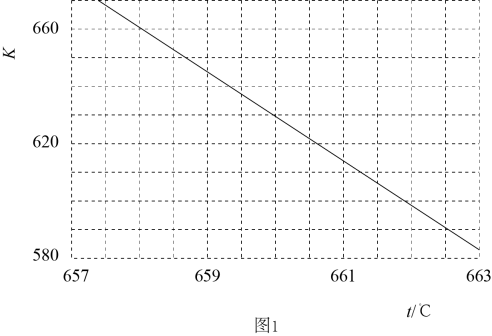
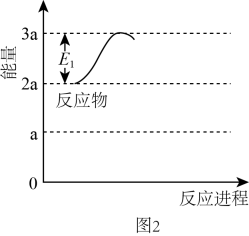
光气(COCl2)是一种重要的化工原料,用于农药、医药、聚酯类材料的生产,工业上通过Cl2(g)+CO(g)⇌COCl2(g)制备.图1为此反应的反应速率随温度变化的曲线,图2为某次模拟实验研究过程中容器内各物质的浓度随时间变化的曲线.回答下列问题:
(3)
利用氨水可以将SO2和NO2吸收,原理如图3所示:NO2被吸收的离子方程式是.
(4)
用粗硅作原料,熔融盐电解法制取硅烷原理如图4,判断B为电源的极,电解时阳极的电极反应式为.
已知:CO2(g)+3H2(g)═CH3OH(g)+H2O(l)△H=﹣akJ•mol﹣1;
2H2(g)+O2(g)═2H2O(l)△H=﹣b kJ•mol﹣1;
CH3OH(g)═CH3OH(l)△H=﹣c kJ•mol﹣1;
则表示CH3OH(l)燃烧热的热化学方程式为:.

①0~6min内,反应的平均速率v(Cl2)=;
②10min改变的条件是,该反应平衡常数变化的趋势是(填“增大”、“减小”或“不变”).


【考点】
化学平衡的计算;
能力提升
真题演练
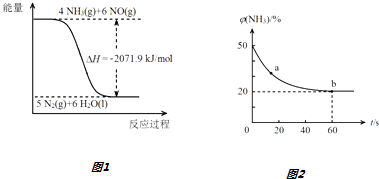


 .实验测得N﹣N键的键能为167kJ•mol﹣1 , NO2中氮氧键的键能为 466kJ•mol﹣1 , N2O4中氮氧键的键能为438.5kJ•mol﹣1 .
.实验测得N﹣N键的键能为167kJ•mol﹣1 , NO2中氮氧键的键能为 466kJ•mol﹣1 , N2O4中氮氧键的键能为438.5kJ•mol﹣1 .