1.
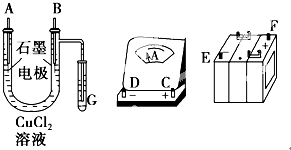
某化学兴趣小组用如图装置电解CuSO4溶液,测定铜的相对原子质量.

(1)
若实验中测定在标准状况下放出的氧气的体积VL,B连接直流电源的 (填“正极”或“负极”),并写出B极发生反应的电极反应式.
(2)
电解开始一段时间后,在U形管中可观察到的现象.
(3)
实验中还需测定的数据是(填写序号).
(4)
铜的相对原子质量为:(用含有m、V的计算式表示).
(5)
如果用碱性(KOH为电解质)甲烷燃料电池作为电源进行实验,放电时负极的电极反应式为.
并写出该电解反应总的离子方程式.
①A极的质量增重mg ②B极的质量增重mg
【考点】
电解原理;
能力提升
真题演练