1.
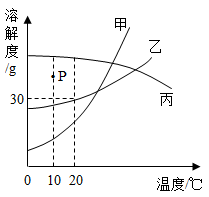
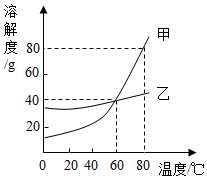
甲、乙、丙三种固体物质的溶解度曲线如图所示,请根据图示回答下列问题.
(1)丙物质的溶解度随温度的升高而(填“增大”或“减小”).
(2)若要从乙物质的饱和溶液中得到乙固体,可用的结晶方法.
(3)t1℃时,将甲物质的饱和溶液升温到t3℃所得溶液中溶质的质量分数(填“变大”、“变小”或“不变”).
(4)t3℃将100g水加入到盛有30g甲物质的烧杯中,充分溶解后得到不饱和溶液,若想使溶液恰好饱和,可采用的方法是:①加入甲物质g; ②降温到℃.
【考点】
固体溶解度曲线及其作用;