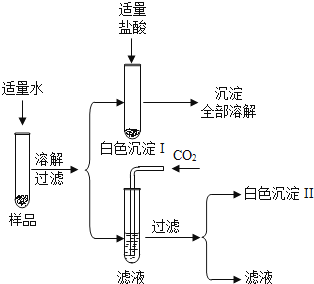
1.
能把MgCl2、KOH、BaCl2三种无色溶液区分开来的一种溶液,有关的化学方程式为;。
【考点】
书写化学方程式、文字表达式;
物质的鉴别、推断;
基础巩固
能力提升
变式训练
拓展培优
真题演练