1.
食盐在生产和生活中具有广泛的用途,是一种重要的资源,海水中储量很丰富.
(1)海水晒盐的原理是;
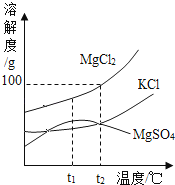
(2)晒盐过程中得到粗盐和卤水.卤水的主要成分及其溶解度的变化如图.t2℃时,MgCl2的溶解度为 100 g;将t2℃时MgCl2、KCl和MgSO4三种物质的饱和溶液分别降温至t1℃时,析出的晶体是 (填物质化学式);
(3)将纯净的氯化钠固体配制成溶液,20℃时,向4个盛有50g水的烧杯中,分别加入一定质量的氯化钠并充分溶解.4组实验数据如下表:
实验序号 | ① | ② | ③ | ④ |
加入氯化钠的质量/g | 4.5 | 9 | 18 | 20 |
溶液质量/g | 54.5 | 59 | 68 | 68 |
若将②中得到的溶液稀释成质量分数为0.9%的生理盐水,需加水的质量是 g.
关于上述实验的叙述不正确的是 (填序号).
A.①②所得溶液是该温度下的不饱和溶液
B.③④所得溶液溶质的质量分数相等
C.20℃时,氯化钠的溶解度为36g
D.20℃时,将④恒温蒸发25g水,过滤得18g固体.
【考点】
固体溶解度曲线及其作用;
晶体和结晶的概念与现象;
溶质的质量分数及相关计算;
用水稀释改变浓度的方法;
粗盐提纯;
基础巩固
能力提升
变式训练