1.
化学小组实验探究  与
与  溶液的反应。
溶液的反应。
(1)
实验一:用如下装置(夹持、加热仪器略)制备  ,将足量
,将足量  通入
通入  溶液中,迅速反应,得到无色溶液A和白色沉淀B。
(2)
对体系中有关物质性质分析得出:沉淀B可能为
溶液中,迅速反应,得到无色溶液A和白色沉淀B。
(2)
对体系中有关物质性质分析得出:沉淀B可能为  、
、  或二者混合物。
(3)
根据沉淀F的存在,推测
或二者混合物。
(3)
根据沉淀F的存在,推测  的产生有两个途径:
(4)
实验一中
的产生有两个途径:
(4)
实验一中  与
与  溶液反应的离子方程式是。
(5)
根据物质性质分析,
溶液反应的离子方程式是。
(5)
根据物质性质分析,  与
与  溶液应该可以发生氧化还原反应。将实验一所得混合物放置一段时间,有Ag和SO42-生成。
溶液应该可以发生氧化还原反应。将实验一所得混合物放置一段时间,有Ag和SO42-生成。
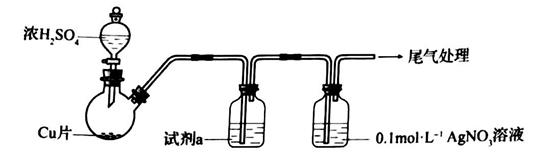
①浓 与Cu反应的化学方程式是
②试剂a是。
(资料: 微溶于水;
难溶于水)
实验二:验证B的成分

①写出 溶于氨水的离子方程式:。
②加入盐酸后沉淀D大部分溶解,剩余少量沉淀F。推断D中主要是 ,进而推断B中含有
。向滤液E中加入一种试剂,可进一步证实B中含有
。所用试剂及现象是。
途径1:实验一中, 在
溶液中被氧化生成
,随沉淀B进入D。
途径2:实验二中, 被氧化为
进入D。
实验三:探究 的产生途径
①向溶液A中滴入过量盐酸,产生白色沉淀,证明溶液中含有;取上层清液继续滴加 溶液,未出现白色沉淀,可判断B中不含
。做出判断的理由:。
②实验三的结论:。
根据上述实验所得结论:。
【考点】
二氧化硫的性质;
硫酸根离子的检验;
含硫物质的性质及综合应用;
能力提升