1.
乙二醇 是应用广泛的化工产品,草酸二甲酯
是应用广泛的化工产品,草酸二甲酯 的热催化加氢是生产乙二醇、乙醇酸甲酯
的热催化加氢是生产乙二醇、乙醇酸甲酯 的重要工艺。主要反应如下:
的重要工艺。主要反应如下:
I.
Ⅱ.
Ⅲ.
(1)
写出由草酸二甲酯热催化加氢生成乙二醇的热化学方程式:。
(2)
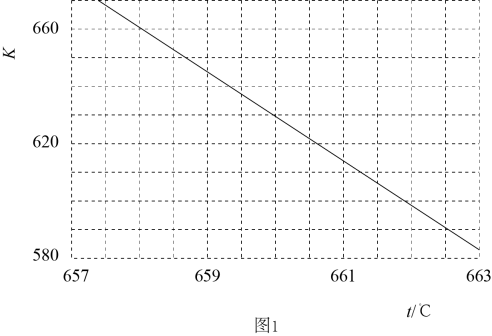
计算表明,反应Ⅲ在研究的温度范围内平衡常数大于 , 可以认为反应Ⅲ几乎不可逆,为了限制反应Ⅲ对乙二醇产率的影响,可采取的最佳措施是___________。
A.
升高反应体系的温度
B.
适当增大反应投料中氢气的比例
C.
增大反应体系的压强
D.
选择合适的催化剂进行反应
(3)
在选定催化剂后,科研人员研究了投料比和压强对反应平衡的影响,测得在
, 可以认为反应Ⅲ几乎不可逆,为了限制反应Ⅲ对乙二醇产率的影响,可采取的最佳措施是___________。
A.
升高反应体系的温度
B.
适当增大反应投料中氢气的比例
C.
增大反应体系的压强
D.
选择合适的催化剂进行反应
(3)
在选定催化剂后,科研人员研究了投料比和压强对反应平衡的影响,测得在 、
、 的等温等压条件下,原料草酸二甲酯的转化率(
的等温等压条件下,原料草酸二甲酯的转化率( )及产物的选择性(S)随投料比的变化关系如图(
)及产物的选择性(S)随投料比的变化关系如图( 生成某产物的草酸二甲酯的物质的量/参与反应的草酸二甲酯的总物质的量)。
(4)
在等压
生成某产物的草酸二甲酯的物质的量/参与反应的草酸二甲酯的总物质的量)。
(4)
在等压 、投料比为50的条件下,科研人员测量了原料草酸二甲酯的转化率(
、投料比为50的条件下,科研人员测量了原料草酸二甲酯的转化率( )及各产物的选择性(S)随温度变化关系,如图。
)及各产物的选择性(S)随温度变化关系,如图。

①当投料比大于80时,乙醇酸甲酯的选择性降低,其原因是。
②已知投料比为60时,草酸二甲酯的转化率为 , 该条件下不发生反应Ⅲ,则最终收集的流出气中甲醇蒸气的分压为
(计算结果保留二位小数)。

①当反应温度高于时,乙二醇的选择性降低,原因是。
②请画出乙醇酸甲酯的产率随温度的变化。
【考点】
化学平衡常数;
能力提升
真题演练