1.
一种在常温、常压下催化电解实现工业合成氨反应的工艺为: ,
,  , 该反应可分两步完成:
, 该反应可分两步完成:
反应Ⅰ:
反应Ⅱ:
请回答下列问题:
(1)

 。
(2)
将
。
(2)
将 和
和 充入到3L的恒容密闭容器中模拟反应Ⅰ:
(3)
从图乙中获知反应Ⅰ存在着高温降低平衡产率与低温降低反应速率等调控矛盾。在提高合成氨的产率的工业生产中,通常从以下多个视角来综合考虑合理的工业生产条件:
(4)
科学家为避免直接破坏
充入到3L的恒容密闭容器中模拟反应Ⅰ:
(3)
从图乙中获知反应Ⅰ存在着高温降低平衡产率与低温降低反应速率等调控矛盾。在提高合成氨的产率的工业生产中,通常从以下多个视角来综合考虑合理的工业生产条件:
(4)
科学家为避免直接破坏 键而消耗大量热能,通过新型催化剂降低了反应路径中决速步的能垒,使该反应在常温、常压下采用电化学方法也能实现,反应装置如图所示:
键而消耗大量热能,通过新型催化剂降低了反应路径中决速步的能垒,使该反应在常温、常压下采用电化学方法也能实现,反应装置如图所示:
①该反应中物质浓度随时间变化的曲线如图甲所示,0~10min内,。
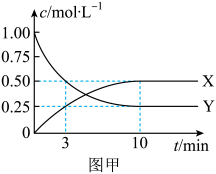
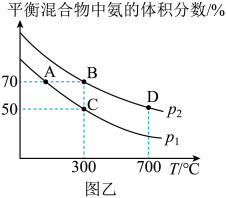
②不同温度和压强下测得平衡时混合物中氨的体积分数与温度的关系如图乙所示,则B、C两点的平衡常数(填“>”、“<”、“=”或“不确定”);B点时
的转化率=(保留2位有效数字)。
反应速率的视角:①加入催化剂;②提高温度(控制在催化剂的活性温度内)
平衡移动和原料的转化率的视角:③,④。
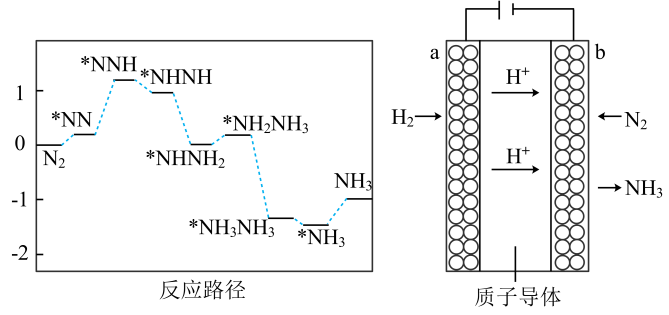
①反应路径中的决速步为 (填写“Ⅰ”、“Ⅱ”、“Ⅲ”或“Ⅳ”) 。
②阴极上的电极反应式为。
【考点】
盖斯定律及其应用;
化学反应速率;
催化剂;
化学平衡移动原理;
化学平衡转化过程中的变化曲线;
电解池工作原理及应用;
能力提升






