1.
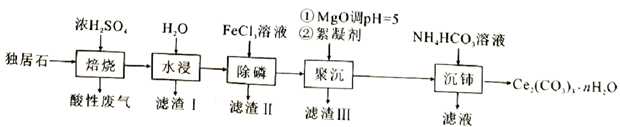
锰酸锂(LiMn2O4)是锂电池的正极材料,以软锰矿为原料,生产锰酸锂的流程如下:

已知:
①软锰矿的成分如下:
成分 | MnO2 | Fe2O3 | CaO | SiO2 | 其他不反应杂质 |
质量分数 | 69.6% | 7.6% | 5.6% | 9.0% | 8.2% |
②K2MnO4在强碱性溶液(pH大于13.5)中稳定,在酸性、中性和弱碱性环境中会发生歧化反应生成和MnO2。
③苯胺(C6H5NH2)还原性较强,在该条件下可被氧化为硝基苯(C6H5NO2)。
④锰酸锂为灰黑色粉末,离子化合物,易溶于水,难溶于无水乙醇。
(1)
“氧压浸出”的浸出温度为260℃,并维持500r/min的速率搅拌,此时发生的氧化还原反应的化学方程式为。
(2)
“加热溶解”和“除杂”时均要严格控制溶液pH的原因是,“除杂”中加入CaO后,需要适当加热并搅拌的目的是,若此时溶液中c( )=2.5mol/L,则1m3溶液中理论上需要加入的CaO的质量为kg。
(3)
“一系列的操作”是将所得溶液加热浓缩、冷却结晶、过滤、洗涤、干燥,其中洗涤的试剂最好选用___________。
A.
冷水
B.
热水
C.
95%的乙醇溶液
D.
LiOH溶液
(4)
纯度的测定:取0.5800g锰酸锂[Mr(LiMn2O4)=181]样品与稀硝酸和双氧水反应,将Mn元素完全转化为Mn2+ , 除去过量的双氧水,调节pH,滴加指示剂,用浓度为0.3000mol/L的EDTA标准溶液滴定,终点时消耗EDTA标准溶液20.00mL(Mn2+与EDTA反应的化学计量数之比为1:1)
)=2.5mol/L,则1m3溶液中理论上需要加入的CaO的质量为kg。
(3)
“一系列的操作”是将所得溶液加热浓缩、冷却结晶、过滤、洗涤、干燥,其中洗涤的试剂最好选用___________。
A.
冷水
B.
热水
C.
95%的乙醇溶液
D.
LiOH溶液
(4)
纯度的测定:取0.5800g锰酸锂[Mr(LiMn2O4)=181]样品与稀硝酸和双氧水反应,将Mn元素完全转化为Mn2+ , 除去过量的双氧水,调节pH,滴加指示剂,用浓度为0.3000mol/L的EDTA标准溶液滴定,终点时消耗EDTA标准溶液20.00mL(Mn2+与EDTA反应的化学计量数之比为1:1)
①若反应时,N元素的化合价不变,则锰酸锂与稀硝酸和双氧水反应的离子方程式为。
②样品中锰酸锂的纯度为%(保留两位有效数字)。
【考点】
物质的分离与提纯;
制备实验方案的设计;
离子方程式的书写;
能力提升
真题演练