1.
下列实验操作规范且能达到目的是 ( )
目的 | 操作 | |
A | 配制100克36%的浓盐酸 | 将200克18%的秒盐酸加热蒸发 100克水 |
D | 清洗碘升华实验所用试管 | 先用酒精清洗,再用水清洗 |
C | 称取9.2克氢氧化钠固体 | 托盘天平右盘加9克砝码,游码置于0.2克处,左盘加氢氧化钠固体至天平平衡 |
B | 检验溶液中是否含有CO2- | 滴入稀硫酸,将产生的气体通入澄清石灰水中 |
A.
A
B.
B
C.
C
D.
D
【考点】
常见实验操作;
基础巩固
能力提升
变式训练
拓展培优
真题演练





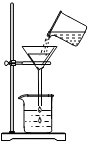

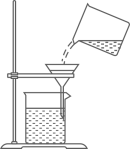 过滤
过滤 点燃酒精灯
点燃酒精灯 闻气味
闻气味









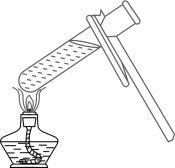
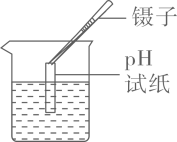




 倾倒液体
倾倒液体 读取体积
读取体积 点燃酒精灯
点燃酒精灯 滴加液体
滴加液体