1.
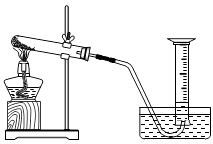
实验室常用MnO2与浓盐酸反应制备Cl2 , 其反应方程式为  反应装置如图1所示(夹持装置已略去)。
反应装置如图1所示(夹持装置已略去)。
(1)
检查装置气密性之后的操作依次是____(选填序号)。
A.
向烧瓶中加入 MnO2粉末
B.
加热
C.
向烧瓶中加入浓盐酸
(2)
制备反应会因盐酸浓度下降而停止。为测定反应残余液中盐酸的浓度,探究小组同学提出下列实验方案:
①甲同学的方案:与足量 AgNO3 溶液反应,称量生成沉淀的质量。此方案(选填“可行”或“不可行”),原因是;
②乙同学的方案:与足量 Zn反应,测量生成的气体体积。实验装置如图2所示(夹持装置已略去)。使 Y形管中的残余溶液与锌粒反应的正确操作是将转移到中。反应完毕,每间隔1分钟读取气体体积,气体体积逐渐减小,直至不变。气体体积逐渐减小的原因是(仪器和实验操作的影响因素除外)。
【考点】
氧气的性质和利用;
制取氧气的原理;
氧气的检验和验满;
能力提升