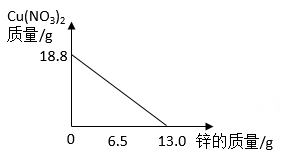
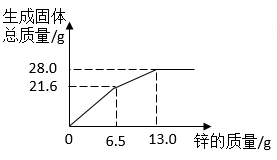
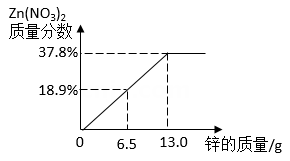
1.
科学兴趣小组做了如下实验:将一镁条放入CuCl2溶液中,镁条表面覆盖了红色物质,但很快镁条表面又冒出很多气泡。他们觉得很奇怪。
【提出问题】这些气泡是怎样产生的? 是什么气体呢?
(1)
【猜想】①是氧气; ②是氯化氢; ③是氨气 (NH3) ;④是氢气。他们马上否定了猜想③,否定的依据是;
(2)
【实验探究】他们开始着手收集所产生的气体。
(3)
【实验结论】
(4)
甲、丙装置中无水硫酸铜的作用是不同的,请指出它们的区别;为确定该气体产生的本质原因,他们用精密pH试纸测试实验所用的(  溶液, pH约为5.5。查阅资料发现:(
溶液, pH约为5.5。查阅资料发现:(  为强酸弱碱盐,其水溶液呈酸性,与实验结果相符。
为强酸弱碱盐,其水溶液呈酸性,与实验结果相符。
实验一:他们用带火星的木条检验该气体,木条不复燃。说明生成的气体不是氧气;
实验二:为继续探究反应后生成的气体是否是氯化氢,他们用检验该气体,试纸不变红,说明生成的气体不是氯化氢;
实验三:为确定气体是否是氢气,他们设计了如图所示的实验 (每个装置的反应均完全) 。

若该气体是氢气,则在乙装置中可以观察到的现象是;
【考点】
金属的化学性质;
能力提升
真题演练