1.
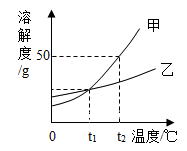
如图是A、B、C三种固体物质的溶解度随温度变化的曲线图.根据图回答:

(1)t3℃时,50g水中加入50gA物质形成溶液的质量为 。
(2)要将t3℃时A B C三种物质的饱和溶液降温到t1℃时三种溶液中溶质的质量分数由大到小的顺序是 。
【考点】
固体溶解度曲线及其作用;
溶质的质量分数及相关计算;