1.
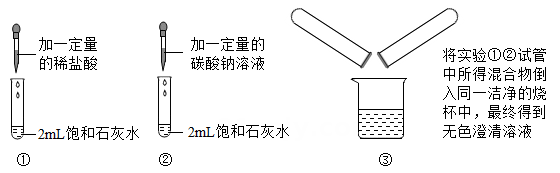
研究小组同学在完成“酸的性质”实验①②后,将①②实验后试管中的物质全部倒入各自废液缸③中(如图甲),结果出现了不同现象,部分小组同学的实验现象记录如下表。

组别 | 废液缸中现象 | 现象解释 |
第1小组 | 无沉淀、有气泡产生 | |
第2小组 | 无沉淀、无气泡产生 | |
第3小组 | … | |
… |
【原理分析】小组同学在老师指导下讨论后认为:任何一个化学反应,反应物的用量不同,反应后物质的组成成分就会不同,这是最终导致各组废液缸中出现不同现象的原因。
(1)
【交流讨论】为分析第1小组废液缸中溶液的溶质成分,用玻璃棒蘸取溶液测得pH=3,则该小组废液中的溶质组成成分为(写化学式),
(2)
如果其他小组实验所用反应物的用量都不一样,除了上面第1、2小组出现的现象外,还会出现的现象是
(3)
【实验拓展】取第1小组废液缸中的溶液于试管中,逐滴加入碳酸钠溶液,并振荡,产生的气体全部逸出。图乙表示“溶液质量”随加入“碳酸钠溶液质量”的变化情况。解释图中AB段和BC段溶液质量呈现不同增加趋势的原因

【考点】
盐的性质及用途;
酸的化学性质;
能力提升
真题演练