1.
草酸亚铁晶体()是生产锂电池电极的原料,它呈浅黄色,难溶于水,受热易分解。某小组设计实验制备草酸亚铁晶体并测定其纯度。
实验(一)制备草酸亚铁晶体并探究其热分解产物。
①称取5.0g , 放入如下图装置的三颈烧瓶中,加入10滴左右1.0mol·L-1硫酸溶液和15mL蒸馏水,加热溶解。

②加入25.0mL饱和草酸溶液(过量),搅拌加热至80~90℃停止加热,静置。
③待浅黄色晶体沉淀后,抽滤、洗涤、干燥得到晶体。
(1)仪器A的作用是________,此实验中三颈烧瓶的规格宜选择________(填字母)。
a.50mL b.100mL c.250mL d.500mL
(2)用98.3%硫酸配制1.0mol·L-1稀硫酸,不需要选用的仪器是_______(填字母)。
| A. | B.  | C.  | D. |
(3)在空气中易变质,可以检验其是否变质的试剂是________(填字母)。
A.苯酚溶液 B.溶液 C.KSCN溶液 D.
溶液
从结构角度分析,其易变质的原因是________。
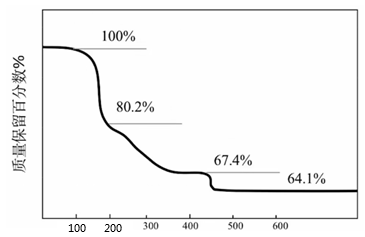
(4)在氩气中,的热重曲线如图所示。已知:
。

推测第二阶段发生反应的化学方程式为________。
实验(二)测定产品纯度。
称取w g产品溶于稀硫酸中,配制成250mL溶液,准确量取25.00mL配制溶液于锥形瓶中,用标准c mol·L-1 KMnO4溶液滴定至终点,消耗滴定液V mL。滴定反应为(未配平)。
(5)该产品含Fe元素质量分数为________(填百分式)。若酸式滴定管没有用待装液润洗,测得结果________(填“偏高”“偏低”或“无影响”)。
【考点】
原子核外电子排布;