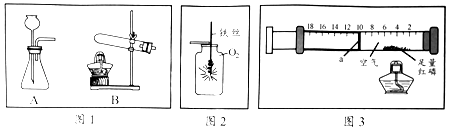
1.
某化学兴趣小组阅读课外资料得知:过氧化氢制氧气除了用二氧化锰作为催化剂,还可以用氧化铜、马铃薯、铁锈、红砖粉末等物质作为催化剂,于是小深想检验生活中的红砖粉末是否能作为过氧化氢分解的催化剂。
【提出问题】红砖粉末是否能作为过氧化氢分解的催化剂?
【猜想】红砖粉末能作为过氧化氢分解的催化剂。
【设计实验】小深同学设计了一系列实验:
实验 | 实验步骤 | 实验现象 |
I | 取5%的过氧化氢溶液5mL于试管中,用带火星的木条伸入试管口 | |
Ⅱ | 取5%的过氧化氢溶液5mL于试管中,加入0.5g红砖粉末,用带火星的木条伸入试管口 | 木条复燃 |
III | 待实验Ⅱ中没有气泡放出后,继续加入5%的过氧化氢溶液,用带火星的木条伸入试管口 |
【实验分析】
(1)
该实验用带火星的木条检验产生的气体,主要是利用氧气具有的性质。
(2)
实验I和III的实验现象分别是。
(3)
实验III重复多次,仍能产生大量气泡,由此可知红砖粉末在反应前后的没有发生改变。
(4)
小圳同学认为小深同学的实验设计不严谨,小圳认为要得出红砖粉末是过氧化氢分解的催化剂,还需要做的实验是:过滤,洗涤,干燥,称量反应后红砖粉末的质量为g。
(5)
【实验结论】红砖粉末可以作为过氧化氢分解的催化剂。
写出用红砖粉末做催化剂分解过氧化氢反应的文字表达式:。
【考点】
氧气的化学性质;
催化剂的特点与催化作用;
能力提升
真题演练