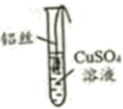
1.
铝、铁、铜是生活中常见的三种金属,请根据金属及性质回答下列问题。
(1)
生活中铝制品比铁制品更耐腐蚀,其原因是。
(2)
某同学用未知金属M进行了以下实验,实验流程及现象如下图所示:(注:M在化合物中化合价为“+2”,题中M的化合物的溶液呈无色)

①写出步骤②中使溶液变蓝的化学反应方程式。
②蓝色滤液中一定含有溶质是(填化学式)。以上实验可得出M、Cu、Ag三种金属活动性的强弱关系是。
【考点】
金属的化学性质;
金属活动性顺序及其应用;