1.
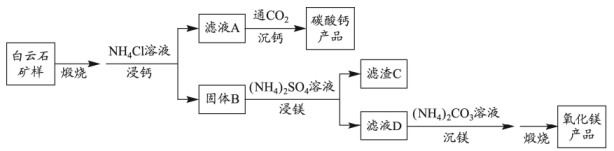
镍及其化合物用途广泛。某矿渣的主要成分是NiFe2O4(铁酸镍)、NiO、FeO、CaO、SiO2等,以下是从该矿渣中回收NiSO4的工艺路线:

已知:①(NH4)2SO4在350℃以上会分解生成NH3和H2SO4 , NiFe2O4在焙烧过程中生成NiSO4、Fe2(SO4)3。②铁元素以针铁矿(FeOOH)形式沉淀,铁渣易过滤。
请回答下列问题:
(1)
焙烧前将矿渣与(NH4)2SO4混合研磨,混合研磨的目的是,写出焙烧过程中铁酸镍发生的化学反应方程式。
(2)
“浸渣”的主要成分为(填化学式)。
(3)
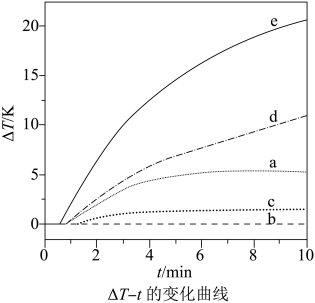
溶液pH对铁去除率的影响实验结果如图所示:
(4)
若溶液中c(Ca2+)=1.0×10-3mol•L-1 , 当除钙率达到99%时,溶液中c(F—)=mol•L-1。[已知Ksp(CaF2)= 4.0×10-11]

①从图中数据来看,沉铁的最佳pH为。
②结合图中数据,解释pH偏小或偏大都不利于沉铁的原因是、。
③检验“除铁”后溶液中是否还有Fe3+的操作是。
【考点】
难溶电解质的溶解平衡及沉淀转化的本质;
能力提升
真题演练