1.
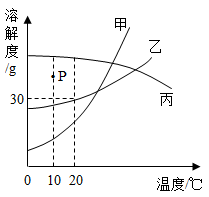
甲、乙物质的溶解度曲线如图所示,请回答下列问题。

(1)
P点表示的含义是。
(2)
t2℃时、将30g甲物质加入50g水中,充分溶解后,所得溶液中溶质的质量分数是(精确到0.1%)。
(3)
t2℃时,取等质量的甲、乙两种物质的饱和溶液,分别恒温蒸发等质量的水后。下列说法正确的是____(填字母)。
A.
溶液中溶剂的质量:甲=乙
B.
析出晶体的质量:甲>乙
C.
若降温到t1℃时,溶液的质量:甲>乙
D.
若降温到t1℃时,溶液中溶质的质量分数:甲=乙
【考点】
固体溶解度曲线及其作用;
能力提升
真题演练