1.
铁、碳可形成许多结构和性质特殊的物质。回答下列问题:
(1)
铁位于元素周期表区;基态Fe原子的价层电子排布图为。
(2)
羰基铁[ ]熔点-20℃,沸点103℃,其结构和部分键长如图1所示。
]熔点-20℃,沸点103℃,其结构和部分键长如图1所示。 晶体类型为晶体,其中含有
晶体类型为晶体,其中含有 键与
键与 键的数目之比为。
(3)
物质磁性大小用磁矩
键的数目之比为。
(3)
物质磁性大小用磁矩 表示,
表示, 与未成对电子数间的关系为:
与未成对电子数间的关系为: (n为未成对电子数)。
(n为未成对电子数)。 的磁矩
的磁矩 ,
,  中氧的孤电子对填入中心离子的 (填标号)杂化轨道形成配位键。
A.
中氧的孤电子对填入中心离子的 (填标号)杂化轨道形成配位键。
A.
 B.
B.
 C.
C.
 D.
D.
 (4)
配合物
(4)
配合物 中配离子
中配离子 的
的 , 则配离子的空间构型为(填“正四面体”或“平面四边形”)。
(5)
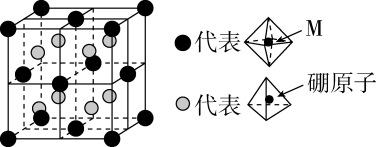
已知石墨晶体的一个六方晶胞如图2所示,晶胞内N点碳的原子坐标。已知石墨层间距334.8pm,C-C键长142pm,计算石墨晶体密度
, 则配离子的空间构型为(填“正四面体”或“平面四边形”)。
(5)
已知石墨晶体的一个六方晶胞如图2所示,晶胞内N点碳的原子坐标。已知石墨层间距334.8pm,C-C键长142pm,计算石墨晶体密度
 (用含
(用含 的表达式表示)。
的表达式表示)。


【考点】
晶胞的计算;
能力提升
真题演练