1.
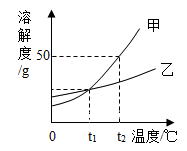
如图是 a、b、c 三种物质的溶解度曲线。

(1)溶液在点 P 时处于(填”饱和”或”不饱和”)状态。
(2)t2℃时,50 克水中最多能溶解 a 物质克。
(3)除去 a 固体中混有的少量 b,提纯的步骤是:加水溶解、 蒸发浓缩、,然后过滤、洗涤、干燥。
(4)t2℃时,将 a、b、c 三种物质的饱和溶液降温至t1℃,下列说法正确的是。
A 溶质质量分数:b > a > c
B 析出固体的质量 a > b,c 无固体析出
C 溶剂的质量:a < b < c
D a、b 是饱和溶液,c 是不饱和溶液。
【考点】
固体溶解度曲线及其作用;
溶质的质量分数及相关计算;