1.
Fe3O4是合成氨催化剂的主要成分。铁泥(主要成分为Fe2O3、FeO,含少量Fe)制备Fe3O4的主要流程如下。

查阅资料:
部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
阳离子 | Mg2+ | Fe2+ | Fe3+ |
开始沉淀时的pH | 9.1 | 7.6 | 1.9 |
沉淀完全时的pH | 11.1 | 9.7 | 3.2 |
请回答下列问题:
(1)
加入H2O2 , 将部分FeSO4转化为Fe2(SO4)3.“氢化”时温度不宜太高,原因是。
(2)
“沉淀”时要控制NaOH的量,原因是。
(3)
“转化”时生成四氧化三铁的同时还生成一种稀酸,则发生反应的化学方程式为。
(4)
合成氨催化过程中因部分Fe3O4与H2反应使催化剂“失效”。在一定温度下可用O2将其“再生”,原理如图所示。“再生”过程中铁元素的质量分数(选填“变大”“变小”成“不变”)。
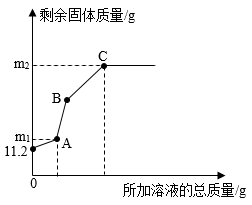
(5)
通入O2加热,将一定质量的失效催化剂进行“再生”,固体质量与温度变化的关系如图所示。T1~T2℃时,FeO转化为Fe3O4 , T3~T4℃时,Fe3O4转化为Fe2O3.则M=。


【考点】
盐的化学性质;
质量守恒定律及其应用;
能力提升
真题演练