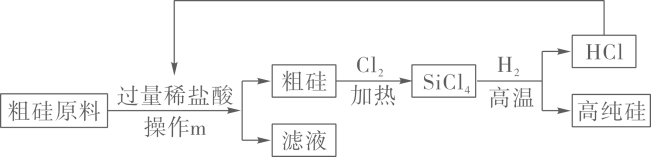
1.
综合题
氨气()是合成氮肥的重要原料,如图1所示是合成氨的新方法。

(1)
ⅰ.传统方法是利用氮气和氢气在高温高压条件下生成氨气,写出该反应的化学方程式为。
(2)
流程中可循环利用的物质是,与传统方法相比,新方法的优点有。
ⅱ.反应器2:常温下,Li与发生的化学方程式为,反应前后氮元素的化合价(填“升高”“降低”或“不变”)。
ⅲ.反应器3:一定条件下,可与
发生反应产生
和氢氧化锂。写出反应的化学方程式为。
ⅳ.氨气产率随反应所用电压的变化如图2所示,电压为V氨气产率最高。
【考点】
有关元素化合价的计算;
化学方程式的书写与配平;
能力提升
真题演练