1.
过碳酸钠(Na2CO4)跟盐酸反应的化学方程式为2Na2CO4+4HCl=4NaCl+2CO2↑+O2↑+2H2O。在过碳酸钠商品中一般都含有 Na2CO3 , 为测定它的纯度,取一定量的样品和盐酸反应,通过测定产生O2的体积,能够运算出Na2CO4的含量。

(1)
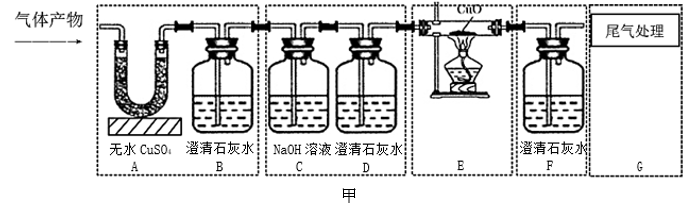
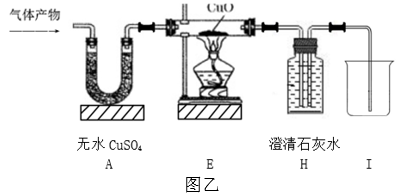
依照如图提供的仪器,组装一套测定商品过碳酸钠尽纯度的实验装置。其中装置④的作用是。
(2)
若在实验中称取1.22g样品进行测定,已知常温下02的密度约为1.42g/L。实验室有50mL、100mL、150mL,三种规格的量筒,该实验所用量筒的规格为,其理由是:。
【考点】
二氧化碳的检验和验满;
真题演练