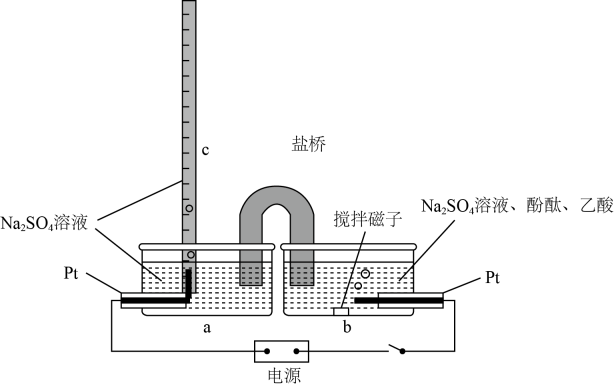
1.
根据原电池的工作原理分析判断(填写“正极”或“负极”)。
(1)
由组成原电池的电极材料判断。一般是活动性较强的金属为极,活动性较弱的金属或能导电的非金属为极。
(2)
根据电流方向或电子流动方向判断。电流由极流向极;电子由极流向极。
(3)
根据原电池中电解质溶液内离子的移动方向判断。在原电池的电解质溶液内,阳离子移向极,阴离子移向极。
【考点】
原电池工作原理及应用;
能力提升
真题演练