1.
某化学兴趣小组的同学围绕“酸碱中和反应”,开展了实验探究活动。
【实验探究】为证明氢氧化钾溶液与稀硫酸发生了反应,三位同学进行了以下实验。
(1)
测定溶液 变化的方法
(2)
测混合过程中的温度变化
(3)
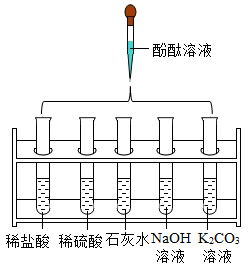
借助于酸碱指示剂
(4)
【提出问题】针对反应后溶液中溶质成分,大家提出了猜想
(5)
【进行实验】为了验证想,学习小组选用
变化的方法
(2)
测混合过程中的温度变化
(3)
借助于酸碱指示剂
(4)
【提出问题】针对反应后溶液中溶质成分,大家提出了猜想
(5)
【进行实验】为了验证想,学习小组选用 粉末、
粉末、 溶液,进行如下探究:
溶液,进行如下探究:
(6)
【评价与反思】
(7)
方案一中的 粉末可以用下列的某些物质代替,也能得到同样的实验结论。请你选出可用药品的字母序号 ____ 。
A.
粉末可以用下列的某些物质代替,也能得到同样的实验结论。请你选出可用药品的字母序号 ____ 。
A.
 B.
B.
 C.
C.
 D.
D.
 E.
E.

甲同学在实验过程中测得变化如图
所示。
点时,溶液中的溶质是 。
乙同学在实验过程中测得反应混合溶液的温度变化如图所示,说明稀硫酸与氢氧化钾溶液发生的反应是
填“放热”或“吸热”
反应,图
中
点表示的含义是 。
丙同学通过图所示实验,他观察到溶液由 ,也证明氢氧化钾溶液与稀硫酸发生了化学反应,反应的化学方程式为 。
【猜想与假设】
猜想一:只有;猜想二: 。
用化学式填空
实验方案 | 实验操作 | 实验现象 | 小组结论 |
方案一 | 取少量反应后的溶液于试管中,加入 | 黑色固体溶解,溶液变成蓝色 | 猜想二正确 |
方案二 | 取少量反应后的溶液于试管中,滴加 | 猜想一正确 |
【实验结论】通过探究,同学们一致确定猜想二是正确的。
针对上述方案提出疑问,认为方案二是不合理的,理由是 。
【考点】
溶解时的吸热或放热现象;
酸碱指示剂的性质及应用;
中和反应及其应用;
溶液的酸碱性与pH值的关系;
实验步骤的探究;
能力提升