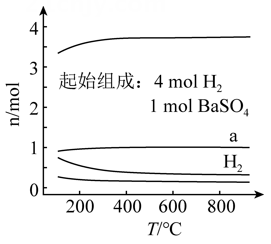
1.
丙烯和卤化氢加成,第一步反应产生的碳正离子中间体有两种可能:
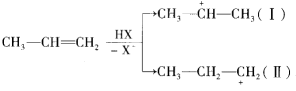
其能量与反应进程关系如图所示。下列说法正确的是( )
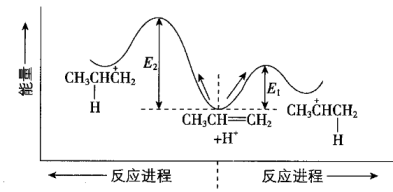
A.
合适的催化剂不能改变E1或E2
B.
碳正离子中间体的稳定性:I>II
C.
碳正离子中间体的生成速率:II<I
D.
由丙烯转化成I和II均要放出热量
【考点】
吸热反应和放热反应;