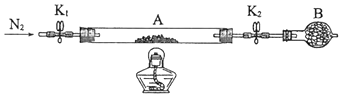
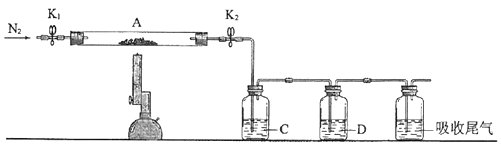
1.
长期放置的FeSO4溶液易被氧化而变质。某兴趣小组分别对新制和久置的两瓶FeSO4溶液进行了如表实验。
(1)
I.分别取2mL新制的FeSO4溶液于三支试管中,进行如图实验。
(2)
方案iii的实验现象是,写出氯水参与反应的的离子方程式:。
(3)
II.久置的FeSO4溶液。
(4)
若要使部分变质的FeSO4复原,发生反应的离子反应方程式是。
(5)
小组同学查阅资料得知,“维生素C可将Fe3+转化为Fe2+”。为了验证维生素C的作用,设计了如表实验vi。
| 实验 | 试剂X | 实验现象 |
实验i | 1mL1mol/LNaOH溶液 | 现象a | |
实验ii | 5滴酸性KMnO4溶液 | 现象b:紫色褪去 | |
实验iii | 依次加入5滴KSCN溶液、5滴氯水 | 现象c |
方案i中,现象a是立即产生白色沉淀,白色沉淀逐渐变为灰绿色,最终变为红褐色。白色沉淀的化学式是,最终变为红褐色的化学方程式是。
实验操作 | 实验现象 | 实验结论 | |
实验iv | 取少量久置的FeSO4溶液于试管中,向其中滴加5滴KSCN溶液 | 溶液变红 | FeSO4溶液部分变质 |
实验v | |||
将上述实验v中的实验操作和现象补充完整。
实验操作 | 实验现象 | |
实验vi | 取一定量Fe2(SO4)3溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性KMnO4溶液 | 紫色褪去 |
由实验vi能否得出“维生素C可将Fe3+转化为Fe2+”的结论?请说明理由。
【考点】
铁盐和亚铁盐的相互转变;
二价铁离子和三价铁离子的检验;
能力提升
真题演练