1.
某实验小组欲探究牺牲阳极法的原理,设计如图实验装置:
(1)
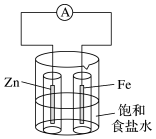
实验Ⅰ:向烧杯中加入一定量的饱和食盐水,插入两个无底玻璃筒。将一根锌棒和一根铁棒用导线与电流表连接后,再分别插入两个玻璃筒中,电流表指针发生偏转。
(2)
向铁棒附近滴加K3[Fe(CN)6]溶液,无明显现象,这说明该实验中无产生。
(3)
实验Ⅱ:该小组的同学将锌棒换为铜棒,并用导线将其与电流表连接。一段时间后,向插入铁棒的玻璃筒内滴入几滴K3[Fe(CN)6]溶液,向插入铜棒的玻璃筒内滴入几滴酚酞溶液。
(4)
在铁棒和铜棒附近可观察到的现象分别是、。
(5)
上述两个实验表明,活泼性不同的两种金属作电极构成原电池时,一般是相对(填“活泼”或“不活泼”)的金属被保护,根据此原理采取的金属防护方法称为。
锌棒上发生的电极反应为;铁棒上发生的电极反应为。
实验Ⅱ中电流表指针的偏转方向与实验Ⅰ(填“相同”或“相反”)。
【考点】
金属的电化学腐蚀与防护;


