1.
二氧化碳与甲烷重整是 利用的研究热点之一、回答下列问题:
利用的研究热点之一、回答下列问题:
(1)
二氧化碳与甲烷重整制CO的反应为:
 (2)
在恒压密闭容器中,起始充入2mol
(2)
在恒压密闭容器中,起始充入2mol (g)和6mol
(g)和6mol (g),发生反应:
(g),发生反应:
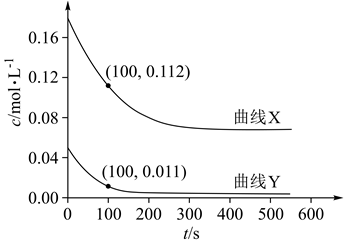
 , 该反应在不同温度下达到平衡时,各组分的体积分数随温度的变化如图所示。
, 该反应在不同温度下达到平衡时,各组分的体积分数随温度的变化如图所示。
已知:
则;若将两等份
和
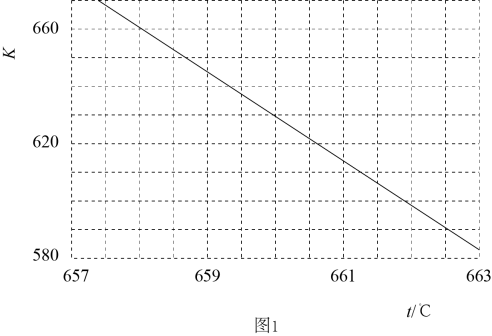
分别充入恒压密闭容器中,在无催化剂和有催化的情况进行反应,相同时间下测得
的转化率与温度的关系如图所示,M点时
转化率相等的主要原因是。


①表示的体积分数随温度变化的曲线是 (填数字序号)。
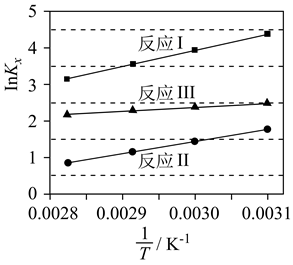
②A、B、C三点对应的化学平衡常数、
、
从大到小的顺序为。
③205℃时,反应达到平衡后,的平衡转化率为 (结果保留一位小数),若平衡时总压为P,平衡常数
(列出计算式。以分压表示,分压=总压×物质的量分数)。
【考点】
化学平衡常数;
化学平衡转化过程中的变化曲线;
能力提升
真题演练







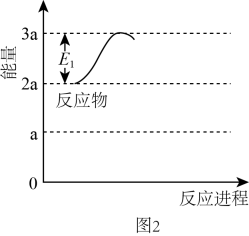
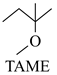 △H1
△H1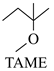 △H2
△H2