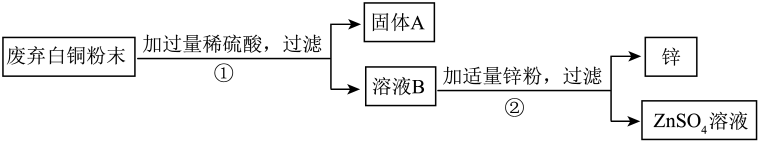
1.
在初中化学“金属的性质”中有如下实验:将无锈铁钉浸入CuSO4溶液,观察到铁钉表面出现红色物质。研究性学习小组对其展开了进一步探究。
(1)
【提出问题】Al和CuSO4溶液也能发生化学反应吗?
(2)
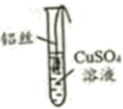
【进行实验】将一端缠绕的铝丝浸入CuSO4溶液(如图),观察现象。
(3)
【实验改进】用砂纸将铝丝表面打磨光亮,将其浸入CuSO4溶液,观察现象。
(4)
【深入探究】为研究上述异常现象,同学们查阅了相关资料,继续开展探究。
(5)
欲加快Al和CuSO4溶液的反应,可加入的物质是。(填一种即可)
(6)
【拓展应用】通过探究,同学们提出了铝制品使用的注意事项。
预测Al能和CuSO4溶液反应,理由是。
铝丝表面未出现红色物质,原因是。
填写实验报告单:
序号 | 实验现象 | 结论与解释 |
① | 铝丝表面有少量气泡;铝丝周围出现蓝绿色物质 | CuSO4溶液呈弱酸性,与Al反应产生的气体是:蓝绿色物质成分待探究 |
② | 24h后,铝丝仍光亮;48h后,铝丝表面出现少量红色物质 | 红色物质是,说明Al能和CuSO4溶液反应,但反应较慢 |
③ | 铝丝周围溶液逐渐变成无色,铝丝以下溶液仍为蓝色;两层溶液界面清晰 | 反应生成的Al2(SO4)3为无色;Al2(SO4)3溶液的密度(填“>” 或“<”)CuSO4溶液 |
资料:①Cu2(OH)2SO4呈蓝绿色,不溶于水;②Cl-可加快铝丝和其他物质的反应速率。
取出铝丝,将试管中的混合物分离得到蓝绿色固体。加入稀硫酸,固体溶解形成蓝色溶液,该反应的化学方程式为。
下列食品不能长时间用铝制炊具盛放的是(填序号)。A.食醋 B.食用油 C.面粉 D.咸菜
【考点】
金属的化学性质;
金属活动性顺序及其应用;
能力提升
真题演练