1.
为纪念门捷列夫发明的元素周期表诞生150周年,联合国大会宣布2019年是“国际化学元素周期表年”。
材料一:门捷列夫将元素按照相对原子质量从小到大排列后,发现元素的化学性质成周期性出现,故将相似化学性质的元素排在同一列。
材料二:门捷列夫无可非议地成为元素周期律的主要发现者,因为门捷列夫的元素周期表有强大的预测功能。
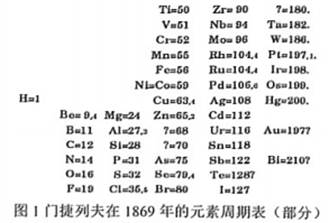
材料三:氟是一种非金属化学元素,氟元素的单质是F2 , 它是一种淡黄色有剧毒的气体。氟气的腐蚀性很强,化学性质极为活泼,是氧化性最强的物质之一。
硫是一种非金属元素,通常单质硫是黄色的品体。硫元素在自然界中通常以化合物或单质的形式存在。硫单质难溶于水,微溶于酒精对人体而言,单质硫通常是无毒无害的。
(1)
根据现代周期表的元素排布特点,下列哪两种元素的化学性质相似?( )
A.
F、Ne
B.
N、O
C.
N、S
D.
N、P
(2)
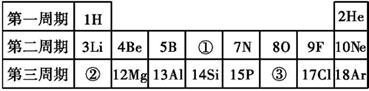
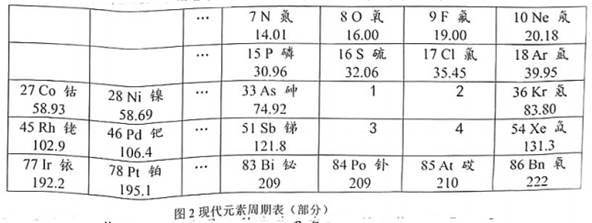
结合材料中图1和图2,现在的元素周期表编制与门捷列夫的元素周期表排列规律有什么相矛盾的地方?
(3)
溴是一种化学元素,相对原子质量是79.9,
溴单质是红黑色液体,溴蒸气具有腐蚀性,并且有毒。请你结合材料预测溴在图2元素周期表中的位置(选择标准序号),并说明理由。
【考点】
元素周期表;
能力提升
真题演练