1.
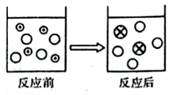
某化学兴趣小组在探究 Mg、Fe、Cu 的性质时进行了如下图所示实验:

(1)
实验一:发生反应的化学方程式;
(2)
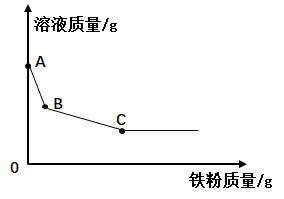
实验二:将实验一后①、②试管内的物质倒入烧杯中,发生烧杯内的红色固体明显增多,一段时间后过滤。滤液中所含金属离子的可能组成有。
①Mg2+、Fe2+、Cu2+ ②Mg2+、Fe3+ ③Mg2+、Fe2+ ④Cu2+、Fe2+
【考点】
金属的化学性质;