1.
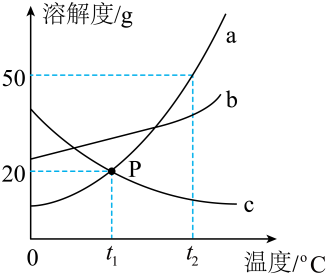
侯德榜先生发明了侯氏制碱法,主要原理及部分操作为:一定条件下,将NH3、CO2通入饱和氯化钠溶液,发生反应:  ,过滤,滤液中主要含有NH4Cl、NaCl两种物质,如图为NH4Cl、NaCl、NaHCO3三种物质的溶解度曲线。回答下列问题:
,过滤,滤液中主要含有NH4Cl、NaCl两种物质,如图为NH4Cl、NaCl、NaHCO3三种物质的溶解度曲线。回答下列问题:

(1)
60℃时,氯化铵的溶解度是g。
(2)
碳酸氢钠晶体首先从溶液中析出的原因是。
(3)
从滤液中得到氯化铵晶体的操作:蒸发浓缩、、过滤、洗涤、干燥。
(4)
将60℃时氯化铵和氯化钠的饱和溶液各100g分别蒸发掉10g水,然后降温至t℃,过滤,得到溶液甲和溶液乙,下列说法正确的是______(填标号)。
A.
甲和乙都是饱和溶液
B.
溶剂的质量:甲<乙
C.
溶液的质量:甲>乙
D.
溶质的质量分数:甲=乙
【考点】
固体溶解度曲线及其作用;
纯碱的制取;
能力提升
真题演练