1.
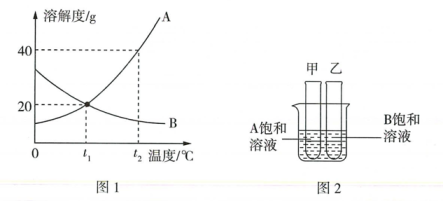
常温下,取100克质量分数为5%的NaCl溶液,先按实验1将NaCl溶液分成两等份,再进行实验2操作,如图所示。

完成下列问题:
(1)
配置100克质量分数为5%的NaCl溶液,不需要用到的仪器是 ;
A.
集气瓶
B.
烧杯
C.
玻璃棒
D.
量筒
(2)
完成实验2操作后,比较甲、乙两只烧杯中溶液的溶质质量分数,其大小关系是(选填“大于”“等于”或“小于”)。
【考点】
溶质的质量分数及相关计算;
一定溶质质量分数的溶液的配制;