1.
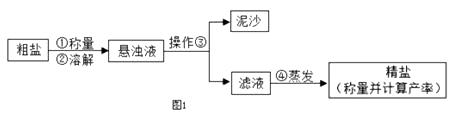
牙膏中常用碳酸钙、二氧化硅等物质作为摩擦剂.某同学对牙膏中摩擦剂碳酸钙的含量进行探究.
【实验原理】测定C装置中生成的BaCO3沉淀的质量,通过计算确定牙膏中CaCO3的质量分数.
【查阅资料】CO2+Ba(OH)2=BaCO3↓+H2O,牙膏中其他成分遇到盐酸时无气体产生.
【实验装置】

根据探究过程回答下列问题:
(1)
装置B中发生反应的化学方程式;
(2)
实验过程中需持续缓缓通入空气,其作用有:①搅拌B、C 中的反应物,使其充分反应;②;
(3)
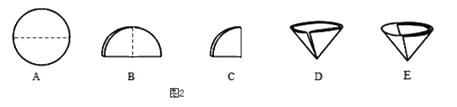
从C中过滤出BaCO3沉淀所需的玻璃仪器有烧杯、和玻璃棒;
(4)
实验中准确称取三份牙膏样品,每份4.0g,进行三次测定,测得生成BaCO3的平均质量为1.97g.则样品中CaCO3的质量分数为;
(5)
若没有A装置,直接通入空气,则测得CaCO3的质量分数(填“偏大”、“偏小”或“不变”).
【考点】
过滤的原理、方法及其应用;
气体的净化(除杂、除水);
盐的化学性质;
实验探究物质的组成成分以及含量;
根据化学反应方程式的计算;