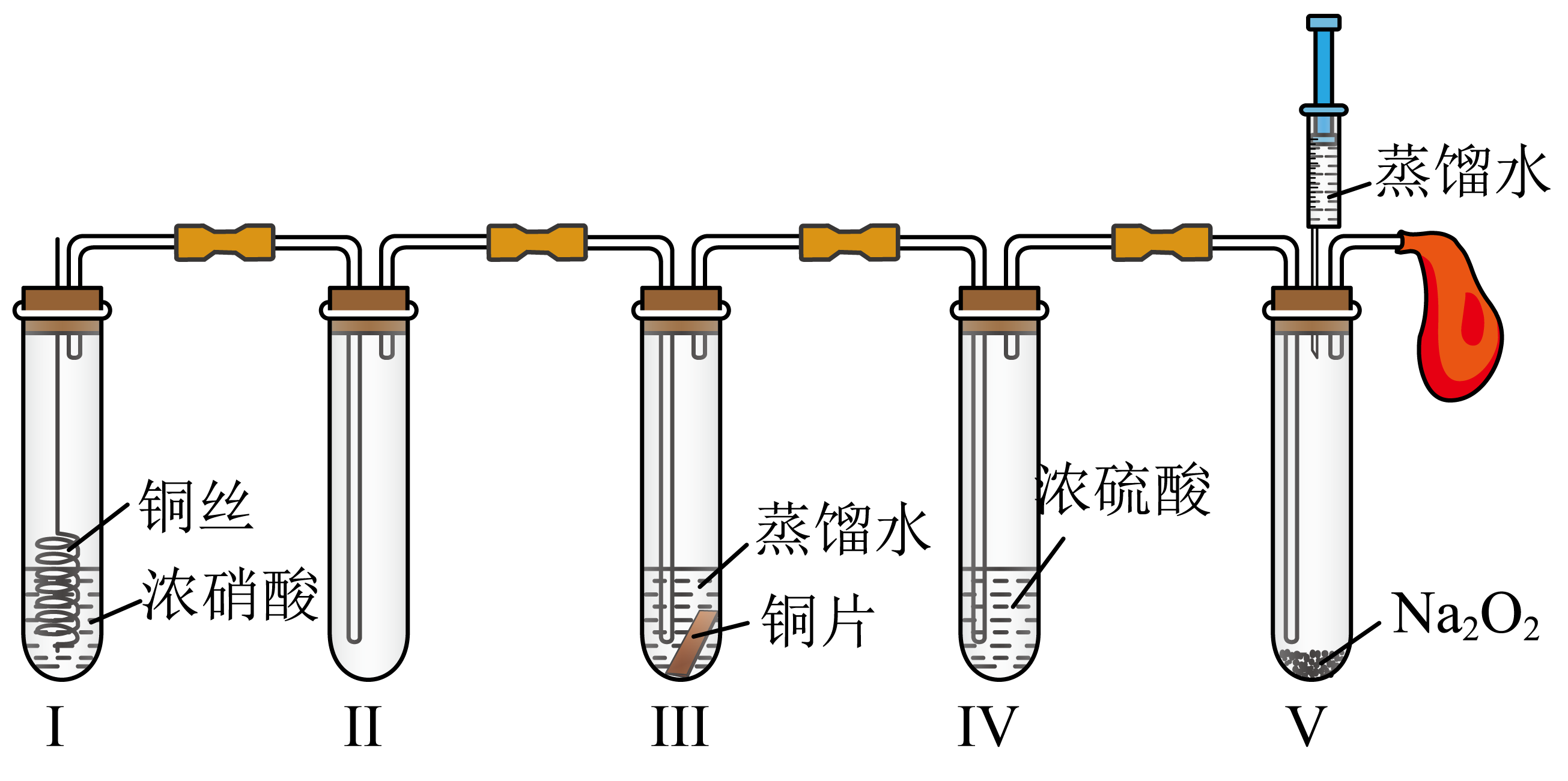
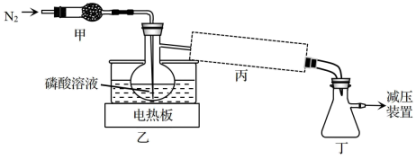
1.
下列有关实验操作、现象和解释或结论都正确的是( )
实验操作 | 现象 | 解释或结论 | |
A | 用试管取2mL溶液,向其中滴入2滴品红溶液,振荡 | 品红溶液褪色 | 该溶液溶有 |
B | 等体积pH=3的HA和HB两种酸分别与足量的锌反应,排水法收集气体 | HA放出的氢气多且反应速率快 | HB酸性比HA强 |
C | 向甲苯中滴入少量浓溴水,振荡,静置 | 溶液分层,上层呈橙红色,下层几乎无色 | 甲苯和溴水发生取代反应,使溴水褪色 |
D | 向尿液中加入新制 | 没有砖红色沉淀生成 | 说明尿液中不含有葡萄糖 |
A.
A
B.
B
C.
C
D.
D
【考点】
物质的分离与提纯;
性质实验方案的设计;
化学实验方案的评价;