1.工业上利用软锰矿(主要成分为 , 含
, 含 等元素)与纤维素制备
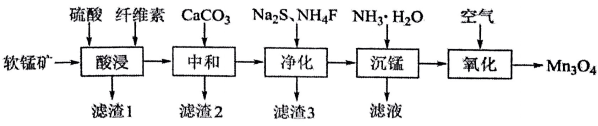
等元素)与纤维素制备 , 工艺如下图所示。
, 工艺如下图所示。
(1)
基态 原子的价电子排布式;为利用纤维素“酸浸”相较于
原子的价电子排布式;为利用纤维素“酸浸”相较于 酸浸法,除了原料来源丰富、耗能低,还具有的优点为.
(2)
“酸浸”时,由纤维素水解得到的葡萄糖与软锰矿反应,该反应的离子方程式为.
(3)
“中和”时,相关离子形成氢氧化物沉淀的
酸浸法,除了原料来源丰富、耗能低,还具有的优点为.
(2)
“酸浸”时,由纤维素水解得到的葡萄糖与软锰矿反应,该反应的离子方程式为.
(3)
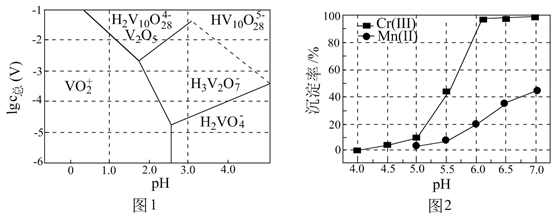
“中和”时,相关离子形成氢氧化物沉淀的 范围如下:
范围如下:
(4)
“净化”时,加入 是为了将
是为了将 转化为
转化为 和
和 沉淀除去,还能除去(填元素符号)。
(5)
“沉锰”时,主要生成
沉淀除去,还能除去(填元素符号)。
(5)
“沉锰”时,主要生成 和
和 沉淀,其中生成
沉淀,其中生成 的离子方程式为.
(6)
“氧化”时,氧化时间对产品中的锰含量及溶液pH的影响如下图。最佳的氧化时间为
的离子方程式为.
(6)
“氧化”时,氧化时间对产品中的锰含量及溶液pH的影响如下图。最佳的氧化时间为 ;下列说法错误的是.
;下列说法错误的是.
金属离子 | |||||
开始沉淀的 | 1.5 | 3.0 | 8.9 | 6.0 | 8.1 |
完全沉淀的 | 2.8 | 4.7 | 10.9 | 8.0 | 10.1 |
“中和”步骤要调节溶液 , 最适宜的
范围是.

A.前 , 主要发生的反应是
下降较慢
B. , 主要发生的反应是
,
下降较快
C.之后,
趋于稳定,则
已完全氧化
D.后,继续通入空气,可能将产品氧化生成
及
, 使产品中锰含量下降
【考点】
原子核外电子排布;
氧化还原反应;
化学反应速率的影响因素;
常见金属元素的单质及其化合物的综合应用;
制备实验方案的设计;
离子方程式的书写;
能力提升
真题演练