1.氧钒(+4价)碱式碳酸铵为紫红色晶体,难溶于水,化学式为(NH4)5[(VO)6(CO3)4(OH)9]∙10H2O,是制备催化剂的基础原料。
(1)
Ⅰ.实验室以VOCl2和NH4HCO3为原料制备氧钒(+4价)碱式碳酸铵晶体的装置如图所示。已知+4价钒的化合物易被氧化。回答下列问题:
(2)
实验步骤①:实验开始时,先(填实验操作),当D中溶液变浑浊,关闭K1 , 进行上述实验操作的目的是。
(3)
若无装置B导致的结果是。
(4)
写出装置C中生成氧钒(+4价)碱式碳酸铵晶体的化学方程式。
(5)
Ⅱ.以V2O5为原料合成该晶体的工艺流程如下图:
(6)
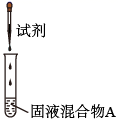
Ⅳ.钒元素的常见离子有V2+、V3+、VO2+、 , 某同学用如图装置验证氧化性
, 某同学用如图装置验证氧化性 强于V3+。
(7)
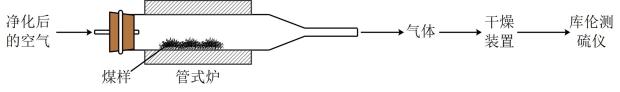
Ⅲ.测定粗产品[氧钒(+4价)碱式碳酸铵晶体]中钒的含量。实验步骤如下:称量a g产品于锥形瓶中,用25.00mL蒸馏水与35mL稀硫酸溶解后,加入0.02mol/L KMnO4溶液至稍过量,充分反应后继续滴加1.5%的NaNO2溶液至稍过量,再用尿素去除过量NaNO2 , 滴入几滴铁氰化钾溶液,最后用0.15 mol/L (NH4)2Fe(SO4)2标准溶液滴定,滴定至终点消耗标准溶液的体积为b mL。产品中钒的质量分数为%(提示:滴定反应为
强于V3+。
(7)
Ⅲ.测定粗产品[氧钒(+4价)碱式碳酸铵晶体]中钒的含量。实验步骤如下:称量a g产品于锥形瓶中,用25.00mL蒸馏水与35mL稀硫酸溶解后,加入0.02mol/L KMnO4溶液至稍过量,充分反应后继续滴加1.5%的NaNO2溶液至稍过量,再用尿素去除过量NaNO2 , 滴入几滴铁氰化钾溶液,最后用0.15 mol/L (NH4)2Fe(SO4)2标准溶液滴定,滴定至终点消耗标准溶液的体积为b mL。产品中钒的质量分数为%(提示:滴定反应为 )。
)。

仪器X的名称为,橡皮管的作用为。
实验步骤②:打开K2 , 滴入溶液,开始反应。

已知N2H4为二元弱碱,N2H4与盐酸反应生成的产物N2H5Cl属于(填“正盐”、“酸式盐”或“碱式盐”)。制备VOCl2溶液时,如不加N2H4也能制备VOCl2溶液,则该反应的离子方程式为。

接通电路后,乙装置的现象是﹔正极的电极反应为。
【考点】
氧化还原反应;
探究物质的组成或测量物质的含量;
制备实验方案的设计;
原电池工作原理及应用;
能力提升
真题演练