1. 葡萄糖→乙醇
葡萄糖→乙醇 乙酸乙酯,根据转化关系判断下列说法正确的是( )
乙酸乙酯,根据转化关系判断下列说法正确的是( )
A.
 可以是淀粉或纤维素,两者互为同分异构体
B.
可以利用银镜反应证明反应①的最终产物为葡萄糖
C.
将烧黑的铜丝趁热插入乙醇中可得到乙醛
D.
乙酸乙酯属于油脂
可以是淀粉或纤维素,两者互为同分异构体
B.
可以利用银镜反应证明反应①的最终产物为葡萄糖
C.
将烧黑的铜丝趁热插入乙醇中可得到乙醛
D.
乙酸乙酯属于油脂
【考点】
同分异构现象和同分异构体;
酯的性质;
葡萄糖的银镜反应;
基础巩固
能力提升
变式训练
拓展培优
真题演练




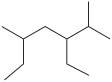 的名称为2,5-二甲基-3-乙基庚烷
的名称为2,5-二甲基-3-乙基庚烷





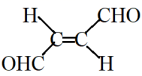
 , R为H或其它基团)易被氧化。
, R为H或其它基团)易被氧化。 和
和 的合成路线流程图(无机试剂及有机溶剂任用,合成路线流程图示例见本题题干)。
的合成路线流程图(无机试剂及有机溶剂任用,合成路线流程图示例见本题题干)。
 )脱氢的反应机理如下。
)脱氢的反应机理如下。