1.一种以硼镁石[主要含 , 还含有少量
, 还含有少量 ]为原料制取
]为原料制取 的工艺流程如下:
的工艺流程如下:
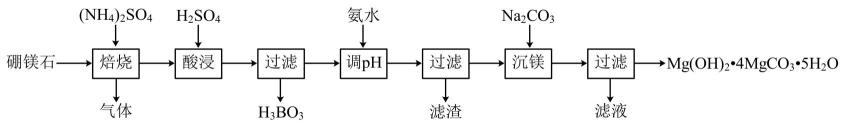
(1)
 与
与 焙烧时生成
焙烧时生成 、
、 、
、 、
、 、
、 和
和 。写出焙烧时
。写出焙烧时 发生反应的化学方程式:。
(2)
由于部分铵盐的分解,焙烧反应所得的气体中除
发生反应的化学方程式:。
(2)
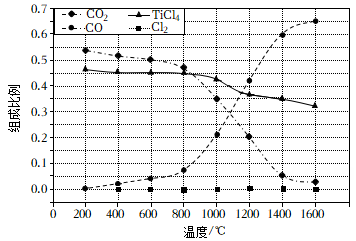
由于部分铵盐的分解,焙烧反应所得的气体中除 和
和 外,还可能含有
外,还可能含有 和
和 , 其中
, 其中 和
和 的体积比为。
(3)
的体积比为。
(3)
 易溶于水,溶于水后生成硼酸
易溶于水,溶于水后生成硼酸 , 硼酸在冷水中溶解度小,溶于水的硼酸可发生电离:
, 硼酸在冷水中溶解度小,溶于水的硼酸可发生电离:


 。硼酸属于元酸。
(4)
用氨水调
。硼酸属于元酸。
(4)
用氨水调 的目的是沉淀
的目的是沉淀 和
和 , 已知实验条件下,部分金属离子开始沉淀的
, 已知实验条件下,部分金属离子开始沉淀的 和对应氢氧化物的
和对应氢氧化物的 如下表所示;溶液中金属离子浓度
如下表所示;溶液中金属离子浓度 , 可以认为沉淀完全。
, 可以认为沉淀完全。
(5)
取 加热分解,所得残留固体的质量与温度的关系如下图所示。
加热分解,所得残留固体的质量与温度的关系如下图所示。 时所得固体的成分为。
时所得固体的成分为。

开始沉淀的 | 8.6 | 3.7 | 2.2 |
氢氧化物的 |
调时需控制的范围是。

【考点】
弱电解质在水溶液中的电离平衡;
制备实验方案的设计;
化学式及其计算;
能力提升
真题演练