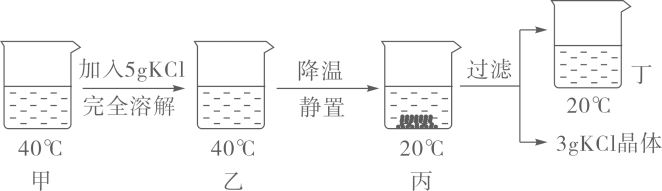
1.20℃时KCl的溶解度是34g。取65gKCl溶液放入甲烧杯中,按如图所示进行操作(整个过程中无溶剂损失)。以下说法正确的是( )
A.
甲烧杯中是KCl的饱和溶液
B.
乙和丙烧杯中KCl的质量分数相等
C.
丁烧杯中KCl的质量分数为34%
D.
若乙烧杯中溶液恰好饱和,则40℃时KCl的溶解度为40g
【考点】
饱和溶液和不饱和溶液;
固体溶解度的概念;
溶质的质量分数及相关计算;
基础巩固
能力提升
变式训练
拓展培优
真题演练