1.KMnO4是实验室常见的氧化剂,实验室用MnO2等作原料制取少量KMnO4的实验流程如图:
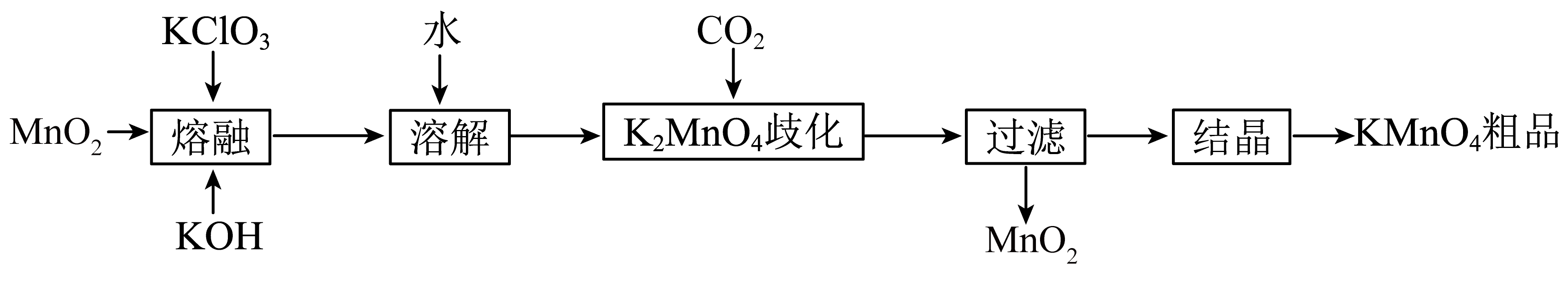
下列说法正确的是( )
A.
“熔融”过程中氧化剂是KClO3 , 还原剂是MnO2
B.
“溶解”后的溶液中存在大量的K+、Cl-、MnO C.
“K2MnO4歧化”时氧化剂与还原剂的分子个数比为1∶2
D.
为了得到更多的晶体,结晶时应大火蒸干
C.
“K2MnO4歧化”时氧化剂与还原剂的分子个数比为1∶2
D.
为了得到更多的晶体,结晶时应大火蒸干
【考点】
氧化还原反应;
制备实验方案的设计;