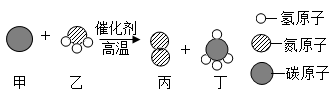
1.某种催化剂可将汽车尾气中的一氧化碳、二氧化氮转化为两种空气中的无毒成分。根据该反应的微观示意图,分析下列说法正确的是( )

A.
四种物质均属于化合物
B.
生成丙和丁的质量比为22:7
C.
参加反应的甲和乙的分子个数比为 1:2
D.
物质丙由原子构成
【考点】
分子、原子、离子、元素与物质之间的关系;
微粒观点及模型图的应用;
根据化学反应方程式的计算;
单质和化合物;
基础巩固
能力提升
变式训练
拓展培优
真题演练