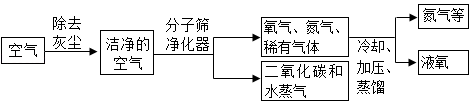
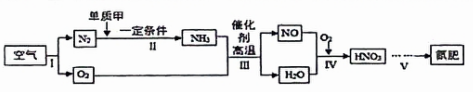
1.空气是宝贵的自然资源,下图是以空气等为原料合成氮肥的流程。
(1)
从物质分类的角度:空气属于(填“混合物”或“纯净物”)。
(2)
从变化角度:步骤1发生的是变化(填“物理”或“化学”),流程图步骤Ⅲ的化学方程式为。
(3)
从守恒角度:“单质甲”为(填写名称)。
(4)
从环保角度:下列保护空气措施不合理的有____(填字母序号)。
A.
工厂通过加高烟囱直接排放废气
B.
提倡步行、骑自行车等“低碳”出行方式
C.
及时清理和妥善处置工业、生活和建筑废渣,减少地面扬尘
【考点】
空气的污染与防治;
物理变化、化学变化的特点及其判别;
化学方程式的书写与配平;
物质的相互转化和制备;
能力提升
真题演练