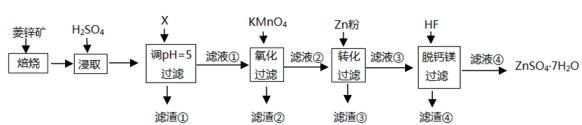
1.油气开采、石油化工、煤化工等行业废气普遍含有的硫化氢,需要回收处理并加以利用。回答下列问题:
(1)
已知下列反应的热化学方程式:
(2)
某恒温恒容条件下,反应④中 的转化率达到最大值的依据是____(填字母)。
A.
气体的压强不发生变化
B.
气体的密度不发生变化
C.
平均摩尔质量不发生变化
D.
单位时间里分解的
的转化率达到最大值的依据是____(填字母)。
A.
气体的压强不发生变化
B.
气体的密度不发生变化
C.
平均摩尔质量不发生变化
D.
单位时间里分解的 和生成的H2的量一样多
(3)
目前较普遍采用的
和生成的H2的量一样多
(3)
目前较普遍采用的 处理方法是克劳斯工艺:
(4)
在1470K、100kPa反应条件下,将
处理方法是克劳斯工艺:
(4)
在1470K、100kPa反应条件下,将 的混合气进行H2S热分解反应。平衡时混合气中H2S与H2的分压相等,H2S平衡转化率为,平衡常数
的混合气进行H2S热分解反应。平衡时混合气中H2S与H2的分压相等,H2S平衡转化率为,平衡常数 kPa(已知:分压=总压×该组分的物质的量分数)。
kPa(已知:分压=总压×该组分的物质的量分数)。
①
②
③
计算热分解反应④
的
kJ/mol,该反应在(填“高温”或“低温”)条件下才可自发进行。
①相比克劳斯工艺,利用反应④高温热分解方法的优缺点是。
②研究人员对反应条件对产率的影响进行了如图研究。同条件下,相同时间内,
产率随温度的变化如图1所示。由图1可见,随着温度升高,
产率先增大后减小,原因是。
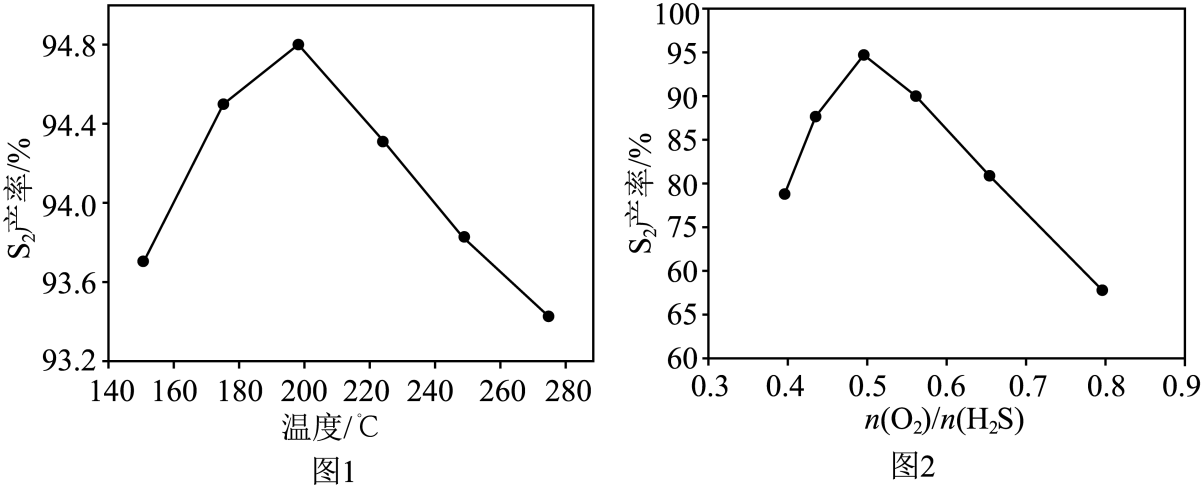
③相同条件下,相同时间内,产率随
值的变化如图2所示。
值过高不利于提高
产率,可能的原因是。
【考点】
盖斯定律及其应用;
化学平衡的影响因素;
化学平衡转化过程中的变化曲线;
化学平衡的计算;
能力提升
真题演练