1.盐酸羟胺 是一种还原剂和显像剂,其化学性质与
是一种还原剂和显像剂,其化学性质与 类似.
类似.
(1)
 被
被 取代可形成羟胺
取代可形成羟胺 , 羟胺水溶液显碱性,用相关离子方程式解释原因.
(2)
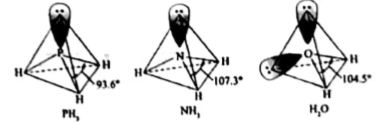
已知氮原子上电子云密度越大则碱性越强,实验测得
, 羟胺水溶液显碱性,用相关离子方程式解释原因.
(2)
已知氮原子上电子云密度越大则碱性越强,实验测得 , 请解释原因:.
(3)
采用原电池原理制备盐酸羟胺的装置如下图所示:
, 请解释原因:.
(3)
采用原电池原理制备盐酸羟胺的装置如下图所示:
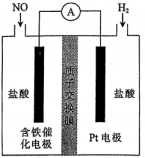
①含铁催化电极发生的电极反应式为.
②盐酸初始浓度相同,假设两侧溶液体积均为且保持不变,理论上电路中通过
电子时,左右两侧
浓度相差
.
【考点】
物质的结构与性质之间的关系;
电极反应和电池反应方程式;
原电池工作原理及应用;
能力提升
真题演练