1.合成氨是人类科学技术上的一项重大突破.
(1)
已知化学键相关数据如下:
(2)
研究表明,合成氨反应在 催化剂上可能通过图1机理进行(
催化剂上可能通过图1机理进行( 表示催化剂表面吸附位,
表示催化剂表面吸附位, 表示被吸附于催化剂表面的
表示被吸附于催化剂表面的 ).判断下述反应机理中,速率控制步骤(即速率最慢步骤)为(填步骤前的标号),理由是.
(3)
为研究温度对合成氨效率的影响,在某温度T下,将一定量
).判断下述反应机理中,速率控制步骤(即速率最慢步骤)为(填步骤前的标号),理由是.
(3)
为研究温度对合成氨效率的影响,在某温度T下,将一定量 和
和 的混合气体置于恒容密闭容器中,在t时刻测得容器中
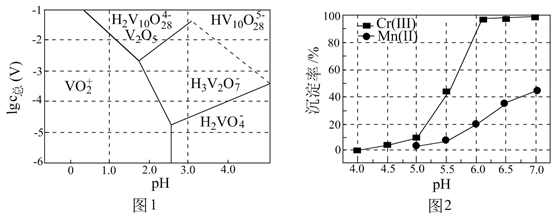
的混合气体置于恒容密闭容器中,在t时刻测得容器中 的物质的量.然后分别在不同温度下,保持其它初始实验条件不变,重复上述实验,经过相同时间测得
的物质的量.然后分别在不同温度下,保持其它初始实验条件不变,重复上述实验,经过相同时间测得 的物质的量.在图2坐标系中,画出
的物质的量.在图2坐标系中,画出 随温度变化的曲线示意图.
(4)
在不同压强下,以两种不同组成进料,反应达平衡时氨的摩尔分数与温度的计算结果如下图所示.其中一种进料组成为
随温度变化的曲线示意图.
(4)
在不同压强下,以两种不同组成进料,反应达平衡时氨的摩尔分数与温度的计算结果如下图所示.其中一种进料组成为 , 另一种为
, 另一种为 . (物质i的摩尔分数:
. (物质i的摩尔分数: 总)
总) D.
进料组成中含有惰性气体
D.
进料组成中含有惰性气体 的是图3
(5)
某温度下,进料组成为
的是图3
(5)
某温度下,进料组成为 , 保持体系压强
, 保持体系压强 不变,当反应达到平衡时测得
不变,当反应达到平衡时测得 , 则该温度下反应
, 则该温度下反应 的
的
 . (
. ( 表示用平衡分压代替平衡浓度求得的平衡常数,分压
表示用平衡分压代替平衡浓度求得的平衡常数,分压 总压
总压 气体的摩尔分数)
气体的摩尔分数)
化学健 | |||
键能 | 436 | 946 | 391 |
, 该反应自发进行的条件是.
(i) (ii)
(iii)
(iv) (v)
图1 反应机理

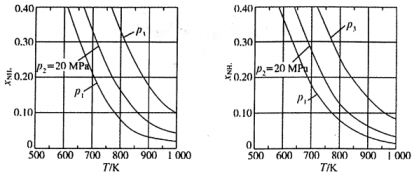
图3 图4
下列说法中不正确的是____:
A. 当氨气的体积分数保持不变时可以判断反应已达平衡 B. 低温高压有利于提高合成氨的平衡产率 C. 压强由大到小的顺序为【考点】
活化能及其对化学反应速率的影响;
焓变和熵变;
化学反应速率的影响因素;
化学平衡的影响因素;
化学平衡的计算;
能力提升
真题演练