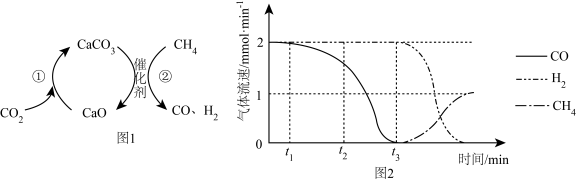
1.在3个容积均为 的恒容密闭容器中分别充入
的恒容密闭容器中分别充入 和
和 , 在不同条件下发生反应:
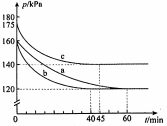
, 在不同条件下发生反应: . 各容器内气体总压强随时间变化如图所示(反应前后容器的温度保持不变).下列说法不正确的是( )
. 各容器内气体总压强随时间变化如图所示(反应前后容器的温度保持不变).下列说法不正确的是( )
A.
与实验a相比,b改变的条件是加入催化剂
B.
与实验a相比,c改变的条件是升温
C.
实验a中 的平衡转化率为
的平衡转化率为 D.
D.

【考点】
化学平衡的影响因素;
化学平衡转化过程中的变化曲线;